-
¿Con qué frecuencia debo realizarme una mastografía después de los 40?
SRC:SelfWritten
 La mastografía es una herramienta fundamental para la detección temprana del cáncer de mama, especialmente en mujeres mayores de 40 años. A medida que se incrementa el riesgo de desarrollar esta enfermedad con la edad, es esencial establecer una periodicidad adecuada para los estudios de imagen. Este artículo aborda las recomendaciones médicas sobre la frecuencia ideal para realizarse una mastografía después de los 40, considerando factores de riesgo y las últimas guías clínicas.
La mastografía es una herramienta fundamental para la detección temprana del cáncer de mama, especialmente en mujeres mayores de 40 años. A medida que se incrementa el riesgo de desarrollar esta enfermedad con la edad, es esencial establecer una periodicidad adecuada para los estudios de imagen. Este artículo aborda las recomendaciones médicas sobre la frecuencia ideal para realizarse una mastografía después de los 40, considerando factores de riesgo y las últimas guías clínicas.
La importancia de la mastografía a partir de los 40 años
El cáncer de mama es una de las principales causas de mortalidad en mujeres, pero las probabilidades de éxito en el tratamiento aumentan significativamente cuando se detecta en etapas iniciales. A partir de los 40 años, el riesgo de desarrollar esta enfermedad incrementa de forma notable, haciendo indispensable la realización de estudios de imagen periódicos.
La mastografía permite identificar anomalías en el tejido mamario incluso antes de que sean palpables. Esto brinda la oportunidad de iniciar tratamientos menos invasivos y más efectivos, mejorando las tasas de supervivencia. Además, los avances tecnológicos, como la mamografía 3D, han mejorado la precisión del diagnóstico, reduciendo falsos positivos y negativos.
Factores que influyen en la periodicidad de la mastografía
Aunque existen recomendaciones generales, la frecuencia con la que una mujer debe realizarse una mastografía después de los 40 años puede variar según diversos factores individuales. Entre los más relevantes se encuentran:
- Historial familiar: Mujeres con antecedentes familiares de cáncer de mama, especialmente en familiares de primer grado, tienen un mayor riesgo y pueden requerir estudios más frecuentes.
- Mutaciones genéticas: Portadoras de mutaciones en los genes BRCA1 o BRCA2 deben iniciar los estudios antes de los 40 años y realizarlos anualmente.
- Tejido mamario denso: Esta condición, común en mujeres más jóvenes, puede dificultar la detección de anomalías y requerir estudios complementarios como ultrasonidos o resonancias magnéticas.
- Condiciones previas: La presencia de lesiones benignas o antecedentes de cáncer de mama aumenta la probabilidad de desarrollar nuevos tumores, justificando una vigilancia más estricta.
- Estado de salud general: Factores como la menopausia, el uso de terapias hormonales y el estilo de vida también influyen en el riesgo de desarrollar cáncer de mama.
Recomendaciones generales para la frecuencia de la mastografía
Las guías médicas internacionales ofrecen diferentes recomendaciones sobre la frecuencia ideal de la mastografía en mujeres mayores de 40 años. Aunque pueden variar según el país o la institución, las más comunes son:
- Mujeres de riesgo promedio:
- La mayoría de las organizaciones, como la Sociedad Americana del Cáncer, sugiere iniciar las mastografías anuales a los 40 años.
- A partir de los 55 años, pueden realizarse cada dos años si no hay factores de riesgo adicionales.
- Mujeres de alto riesgo:
- Se recomienda comenzar los estudios antes de los 40 años, generalmente entre los 30 y 35 años.
- La periodicidad suele ser anual y puede combinarse con otros métodos diagnósticos, como resonancias magnéticas.
- Mujeres mayores de 75 años:
- La necesidad de continuar con mastografías depende del estado de salud general y la expectativa de vida. Si la paciente goza de buena salud, los estudios pueden mantenerse cada dos años.
Beneficios de realizarse mastografías periódicas después de los 40
La realización regular de mastografías ofrece múltiples beneficios, tanto a nivel diagnóstico como en términos de calidad de vida. Entre los principales se destacan:
1. Detección temprana de cáncer de mama
El cáncer de mama en sus etapas iniciales suele ser asintomático. Las mastografías permiten identificar anomalías pequeñas que no son detectables al tacto, aumentando las posibilidades de un tratamiento exitoso.
2. Reducción de la mortalidad
Los estudios han demostrado que la detección temprana a través de mastografías reduce significativamente las tasas de mortalidad por cáncer de mama, especialmente en mujeres de 50 a 69 años.
3. Tratamientos menos invasivos
Detectar un tumor en sus etapas iniciales permite optar por tratamientos menos agresivos, como cirugías conservadoras o radioterapia localizada, en lugar de mastectomías o quimioterapia extensiva.
4. Monitoreo continuo de la salud mamaria
Las mastografías regulares ofrecen un seguimiento constante, permitiendo a los médicos detectar cambios en el tejido mamario a lo largo del tiempo y actuar de manera oportuna.
Controversias sobre la frecuencia de las mastografías
Aunque las mastografías son esenciales en la prevención del cáncer de mama, existen debates sobre su frecuencia ideal. Algunos especialistas consideran que los estudios anuales pueden generar falsos positivos, aumentando la ansiedad en las pacientes y llevando a procedimientos innecesarios.
Por otro lado, la exposición acumulativa a radiación, aunque mínima, es un tema de preocupación para algunas mujeres. Sin embargo, la tecnología moderna ha reducido significativamente la dosis de radiación utilizada en las mastografías, manteniéndola dentro de los límites seguros.
Además, la periodicidad ideal debe adaptarse a cada paciente. Las guías generales son útiles como referencia, pero es fundamental que cada mujer discuta con su médico cuál es la mejor estrategia de prevención según su historial y estado de salud.
Complementos a la mastografía en la detección temprana
En algunos casos, la mastografía puede no ser suficiente para una evaluación completa, especialmente en mujeres con tejido mamario denso. Para estas pacientes, se recomienda complementar el estudio con otras técnicas de imagen, como:
- Ultrasonido mamario: Ideal para detectar lesiones que pueden no ser visibles en una mastografía, especialmente en mujeres jóvenes.
- Resonancia magnética: Utilizada en pacientes con alto riesgo o antecedentes familiares, ofrece imágenes detalladas del tejido mamario sin exposición a radiación.
- Exámenes clínicos: Realizados por médicos especializados, son útiles para identificar cambios sospechosos en los senos.
Reflexión final
Realizarse una mastografía después de los 40 es una de las estrategias más efectivas para prevenir y detectar el cáncer de mama en etapas tempranas. La periodicidad ideal debe ser determinada de manera personalizada, considerando factores como el historial médico, el riesgo genético y el estado general de salud.
Mientras que las guías médicas sugieren mastografías anuales o bienales, es esencial que cada mujer consulte a su médico para establecer un plan de monitoreo adaptado a sus necesidades. Además, el uso de tecnologías complementarias, como ultrasonidos y resonancias magnéticas, puede mejorar la precisión del diagnóstico y garantizar una evaluación integral.
La detección temprana no solo salva vidas, sino que también mejora significativamente la calidad de vida de las pacientes. Promover la educación y la prevención es clave para reducir la incidencia del cáncer de mama y garantizar que cada mujer reciba la atención adecuada en el momento oportuno.
-
Beneficios de realizarse una mastografía regularmente
SRC:SelfWritten
 La mastografía es una herramienta esencial en la detección temprana del cáncer de mama, una enfermedad que afecta a millones de mujeres en todo el mundo. Realizarse este estudio de forma periódica puede marcar la diferencia entre detectar una anomalía en sus primeras etapas o enfrentar un diagnóstico tardío. Este artículo explora los beneficios de realizarse una mastografía, resaltando su impacto en la prevención y tratamiento de las enfermedades mamarias.
La mastografía es una herramienta esencial en la detección temprana del cáncer de mama, una enfermedad que afecta a millones de mujeres en todo el mundo. Realizarse este estudio de forma periódica puede marcar la diferencia entre detectar una anomalía en sus primeras etapas o enfrentar un diagnóstico tardío. Este artículo explora los beneficios de realizarse una mastografía, resaltando su impacto en la prevención y tratamiento de las enfermedades mamarias.
Detección temprana: un factor clave en la lucha contra el cáncer de mama
Uno de los principales beneficios de realizarse una mastografía es su capacidad para identificar anomalías en el tejido mamario antes de que sean detectables al tacto. Este estudio utiliza tecnología de rayos X para capturar imágenes detalladas de los senos, permitiendo a los especialistas identificar cambios sospechosos, como calcificaciones o masas, incluso en etapas iniciales.
La detección temprana aumenta significativamente las probabilidades de un tratamiento exitoso. Según datos de la Organización Mundial de la Salud (OMS), los tratamientos tienen una tasa de éxito superior al 90% cuando el cáncer de mama se detecta a tiempo. Este porcentaje destaca la importancia de los chequeos regulares de mama para reducir la mortalidad asociada a esta enfermedad.
Prevención de enfermedades mamarias mediante chequeos regulares
Los chequeos regulares de mama, que incluyen la mastografía, son fundamentales no solo para detectar el cáncer, sino también para identificar otras condiciones benignas que pueden afectar la salud mamaria. Entre estas condiciones se encuentran los quistes, los fibroadenomas y las calcificaciones benignas. Aunque no suelen representar riesgos graves, el monitoreo constante es esencial para evitar complicaciones futuras.
Además, someterse a mastografías periódicas fomenta la cultura de la prevención, promoviendo una mayor conciencia sobre la salud mamaria. Este hábito ayuda a las mujeres a familiarizarse con sus cuerpos, a entender los cambios naturales que ocurren con el tiempo y a acudir al médico ante cualquier signo de alarma.
Reducción de tratamientos invasivos y costos médicos
Detectar una enfermedad en su etapa inicial a través de una mastografía puede reducir la necesidad de tratamientos invasivos, como la mastectomía o la quimioterapia. Por ejemplo, un tumor identificado en sus primeras fases es más manejable con procedimientos menos agresivos, como una cirugía conservadora y radioterapia localizada. Este enfoque no solo mejora la calidad de vida de las pacientes, sino que también disminuye los costos asociados al tratamiento.
Por otro lado, los estudios preventivos, como la mastografía, son considerablemente más económicos en comparación con los tratamientos avanzados. Invertir en chequeos regulares de mama se traduce en un ahorro a largo plazo, tanto para los sistemas de salud pública como para las pacientes.
Impacto psicológico de la prevención
El diagnóstico de una enfermedad, especialmente el cáncer, puede ser emocionalmente devastador. Sin embargo, realizarse mastografías de manera periódica ofrece tranquilidad, ya que permite monitorear la salud mamaria de forma proactiva. Las pacientes que se someten a estos estudios regularmente experimentan menos incertidumbre y ansiedad, dado que cuentan con información actualizada sobre su estado de salud.
Además, el acompañamiento médico durante estos chequeos fomenta una relación de confianza entre las mujeres y sus especialistas, fortaleciendo el compromiso con el cuidado de su bienestar. Este aspecto psicológico es tan importante como el físico, ya que contribuye a una mejor calidad de vida.
Mastografía y factores de riesgo: una herramienta personalizada
Otro de los beneficios de realizarse una mastografía regularmente es la posibilidad de adaptar los estudios a las necesidades específicas de cada mujer. Por ejemplo, aquellas con factores de riesgo elevados, como antecedentes familiares de cáncer de mama, mutaciones genéticas o exposición prolongada a estrógenos, pueden requerir un monitoreo más frecuente y detallado.
En estos casos, la mastografía puede complementarse con otros estudios, como resonancias magnéticas o ultrasonidos, para ofrecer una evaluación integral. Este enfoque personalizado asegura que cada paciente reciba la atención adecuada según su perfil de riesgo, optimizando las posibilidades de detección temprana y tratamiento.
Educación y concienciación sobre la salud mamaria
Realizarse mastografías regularmente no solo beneficia a nivel individual, sino que también contribuye a una mayor conciencia colectiva sobre la importancia de la prevención. Muchas campañas de salud pública utilizan este examen como un eje central para promover prácticas de cuidado en las mujeres de todas las edades.
Por ejemplo, el mes de octubre, dedicado a la lucha contra el cáncer de mama, refuerza el mensaje de que los chequeos regulares de mama pueden salvar vidas. Estas iniciativas buscan desmitificar el miedo al diagnóstico y fomentar una cultura de cuidado continuo.
Limitaciones de la mastografía: un análisis crítico
Aunque la mastografía es una herramienta altamente efectiva, es importante reconocer sus limitaciones. En algunos casos, los resultados pueden generar falsos positivos o negativos, lo que puede llevar a procedimientos innecesarios o a la omisión de diagnósticos. Sin embargo, estos riesgos se minimizan significativamente cuando el estudio es interpretado por especialistas capacitados.
Por ello, es fundamental combinar la mastografía con otros métodos de evaluación y mantener un diálogo constante con los profesionales de la salud. Este enfoque integral asegura un diagnóstico más preciso y confiable, maximizando los beneficios del examen.
Reflexión final
Los beneficios de realizarse una mastografía de manera regular son innegables. Este estudio no solo permite la detección temprana del cáncer de mama, sino que también contribuye a la prevención de otras condiciones mamarias, reduce la necesidad de tratamientos invasivos y ofrece tranquilidad emocional. Además, fomenta una cultura de cuidado preventivo que puede salvar vidas.
En un mundo donde el cáncer de mama sigue siendo una amenaza significativa, la mastografía se posiciona como una herramienta esencial para proteger la salud de las mujeres. Priorizar estos chequeos regulares de mama, junto con la adopción de hábitos saludables, es un paso firme hacia un futuro donde la detección oportuna sea la norma y no la excepción.
-
Diferencias entre mastografía digital y analógica
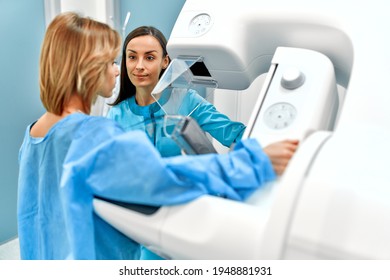 La mastografía es un estudio de imagen esencial para la detección temprana del cáncer de mama y otras patologías mamarias. En los últimos años, la tecnología ha evolucionado, dando lugar a la mastografía digital, que ha reemplazado en muchos casos a la mastografía analógica tradicional. Este artículo analiza las diferencias clave entre ambas técnicas, sus ventajas y desventajas, así como su impacto en la práctica clínica.
La mastografía es un estudio de imagen esencial para la detección temprana del cáncer de mama y otras patologías mamarias. En los últimos años, la tecnología ha evolucionado, dando lugar a la mastografía digital, que ha reemplazado en muchos casos a la mastografía analógica tradicional. Este artículo analiza las diferencias clave entre ambas técnicas, sus ventajas y desventajas, así como su impacto en la práctica clínica.Características de la mastografía analógica
La mastografía analógica, también conocida como convencional, utiliza rayos X para capturar imágenes de los tejidos mamarios. Estas imágenes se imprimen en placas de película radiográfica y requieren un revelado químico para su interpretación. A pesar de ser una tecnología que ha demostrado eficacia durante décadas, presenta limitaciones significativas frente a las opciones modernas.
Ventajas
- Disponibilidad: Amplia implementación en centros de salud, especialmente en regiones con menos recursos.
- Costo inicial bajo: El equipamiento es más económico en comparación con los sistemas digitales.
Desventajas
- Calidad de imagen limitada: Las imágenes tienen menor resolución y contraste, dificultando la detección de lesiones pequeñas o sutiles.
- Procesos más lentos: El revelado de las películas consume tiempo y requiere el uso de productos químicos.
- Conservación de registros: Las películas son propensas a deteriorarse con el tiempo y requieren espacio físico para su almacenamiento.
Características de la mastografía digital
La mastografía digital, por otro lado, captura las imágenes en formato electrónico mediante detectores digitales. Estas imágenes se almacenan en sistemas computarizados, lo que permite su manipulación, análisis y transmisión con facilidad.
Ventajas
- Calidad superior: Las imágenes digitales ofrecen mayor resolución y contraste, facilitando la identificación de microcalcificaciones y otras anomalías.
- Procesamiento rápido: No requiere revelado químico, lo que agiliza la obtención de resultados.
- Almacenamiento eficiente: Los archivos digitales pueden guardarse indefinidamente en sistemas de almacenamiento electrónico.
- Telemedicina: Permite compartir imágenes con especialistas de otros centros para segundas opiniones o evaluaciones complementarias.
Desventajas
- Costo inicial elevado: Los equipos digitales son significativamente más caros que los analógicos.
- Accesibilidad limitada: Su disponibilidad puede ser menor en áreas rurales o en países en desarrollo.
Diferencias clave entre ambas técnicas
La transición de la mastografía analógica a la digital se basa en varias diferencias fundamentales que impactan tanto en la práctica médica como en la experiencia del paciente. Estas diferencias incluyen:
- Resolución de imagen: La mastografía digital proporciona mayor nitidez y detalle, lo que mejora la detección temprana de anormalidades.
- Radiación: Los sistemas digitales suelen utilizar menores dosis de radiación, lo que reduce el riesgo para las pacientes.
- Acceso a los resultados: Las imágenes digitales pueden visualizarse de inmediato, mientras que las analógicas requieren tiempo para el revelado.
- Capacidades de análisis: En la mastografía digital, el uso de software avanzado permite realizar análisis computarizados que aumentan la precisión diagnóstica.
Impacto en la detección temprana del cáncer de mama
La mastografía digital ha demostrado ser más efectiva en ciertos grupos de pacientes, como mujeres jóvenes con tejido mamario denso. El aumento en la sensibilidad y especificidad de esta tecnología contribuye a la detección de lesiones en etapas iniciales, mejorando las tasas de supervivencia y reduciendo la necesidad de tratamientos invasivos.
Sin embargo, es importante destacar que la mastografía analógica sigue siendo una herramienta útil en muchas regiones donde la tecnología digital no está disponible. En estos casos, su implementación adecuada y combinada con programas de educación y seguimiento puede garantizar resultados positivos.
Reflexión final
La evolución de la mastografía analógica a la digital representa un avance significativo en la medicina diagnóstica. Aunque ambas técnicas tienen un papel importante en la detección del cáncer de mama, la mastografía digital ofrece ventajas notables en calidad de imagen, rapidez y eficiencia. No obstante, es crucial garantizar la accesibilidad a estas tecnologías en todas las regiones, promoviendo la equidad en la atención sanitaria y mejorando los resultados clínicos a largo plazo.
-
¿Cuándo es necesario realizarse un electrocardiograma?
SRC:SelfWritten
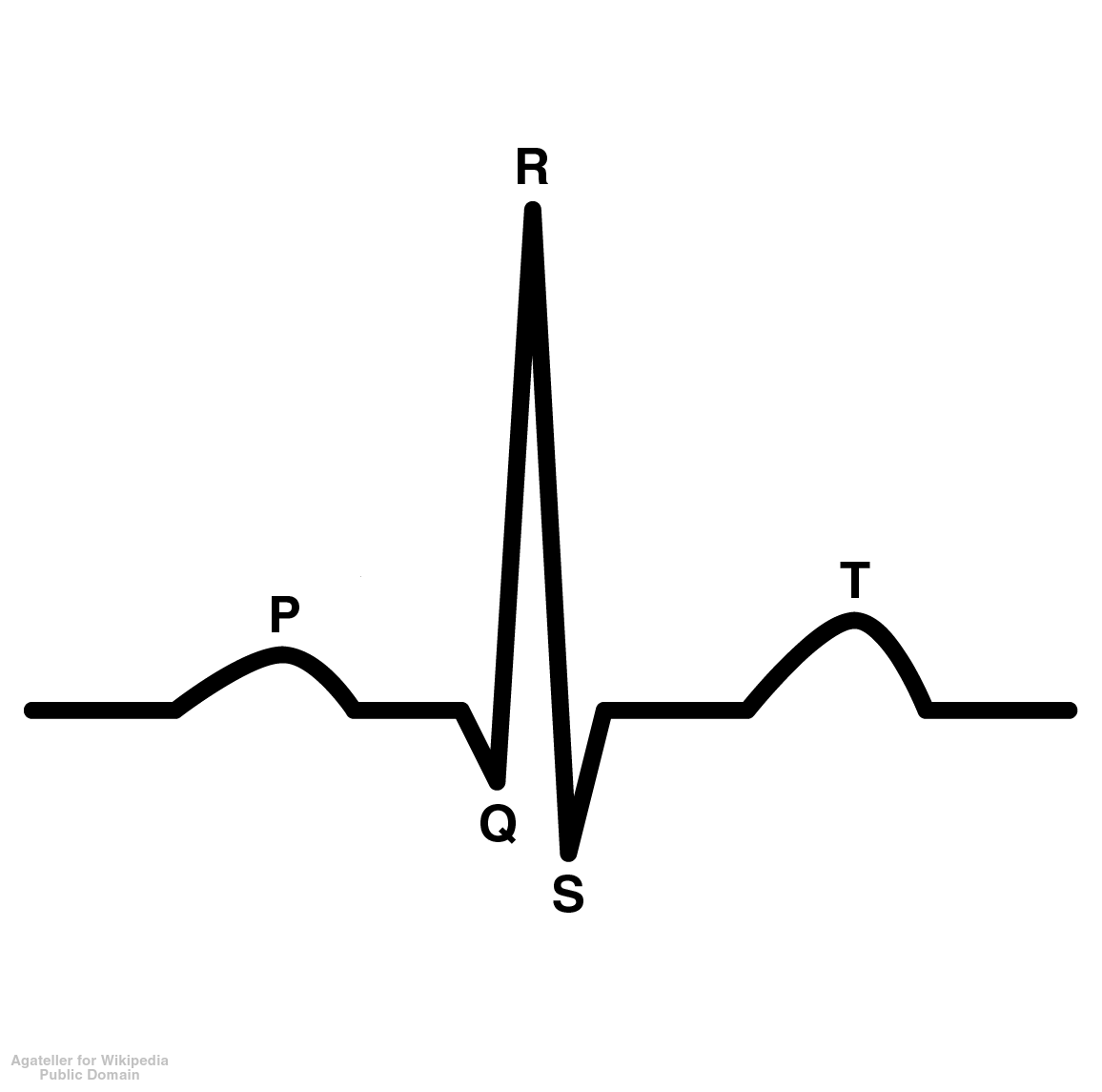
El electrocardiograma (ECG) es una herramienta diagnóstica esencial que permite examinar la actividad eléctrica del corazón. A través de electrodos colocados en la piel, se obtiene un registro visual de los impulsos eléctricos que generan los latidos cardíacos. Sin embargo, muchas personas no saben cuándo realizarse un electrocardiograma. Este procedimiento es crucial para detectar diversas afecciones cardíacas, que en ocasiones pueden no presentar síntomas evidentes. En este artículo, exploraremos las situaciones y los síntomas que indican cuándo realizarse un electrocardiograma, así como las indicaciones para EKG en casos específicos.¿Qué es un electrocardiograma y por qué es importante?
Un electrocardiograma es un examen no invasivo que permite registrar la actividad eléctrica del corazón, facilitando la identificación de trastornos del ritmo, la estructura y el funcionamiento del órgano. Al detectar anomalías en el ritmo cardíaco o signos de daño, el ECG puede ayudar a diagnosticar afecciones como las arritmias, el infarto de miocardio, la hipertensión y otros problemas del corazón.
Aunque el ECG no es una herramienta exclusiva para diagnosticar problemas graves, puede ser fundamental para identificar cambios en el corazón que, si no se tratan a tiempo, pueden dar lugar a complicaciones mayores. Este examen se realiza en condiciones específicas, que van desde chequeos preventivos hasta la evaluación de síntomas relacionados con posibles problemas cardíacos.
Síntomas que sugieren la necesidad de realizarse un electrocardiograma
Existen diversos síntomas que pueden ser indicativos de problemas cardíacos, y en muchos casos, un electrocardiograma puede ser una herramienta esencial para el diagnóstico adecuado. A continuación, se describen algunos de los principales síntomas que pueden requerir la realización de un ECG:
Dolor en el pecho
El dolor en el pecho es uno de los síntomas más comunes que indica cuándo realizarse un electrocardiograma. Este dolor puede ser un signo de un problema grave, como un infarto de miocardio, angina de pecho o pericarditis. Si una persona experimenta dolor en el pecho, especialmente si está acompañado de dificultad para respirar, sudoración excesiva o mareos, es fundamental acudir a un médico de inmediato para obtener un diagnóstico adecuado. Un ECG puede ayudar a determinar si el dolor está relacionado con un trastorno cardíaco.
Dificultad para respirar
La dificultad para respirar o la disnea puede ser un síntoma de diversas afecciones cardíacas, como insuficiencia cardíaca, arritmias o enfermedades de las válvulas cardíacas. Cuando una persona experimenta dificultad para respirar sin una causa clara, como ejercicio intenso o alergias, es recomendable realizarse un electrocardiograma. El ECG puede ayudar a identificar si hay un problema en el corazón que esté afectando la capacidad de bombear sangre de manera eficiente.
Ritmo cardíaco irregular
El ritmo cardíaco irregular, también conocido como arritmia, es otro de los síntomas que indican cuándo realizarse un electrocardiograma. Las arritmias pueden incluir palpitaciones, latidos rápidos o lentos, o una sensación de irregularidad en el latido del corazón. Estas alteraciones del ritmo pueden ser inofensivas o, en casos graves, pueden poner en riesgo la vida del paciente. Un ECG es una herramienta eficaz para identificar la causa de estas irregularidades y determinar si es necesario un tratamiento adicional.
Desmayos o mareos
Los desmayos o mareos recurrentes pueden ser signos de una condición cardíaca subyacente, como arritmias, bloqueo de las arterias coronarias o insuficiencia cardíaca. En estos casos, un electrocardiograma es útil para analizar cómo funciona el corazón y para detectar si hay irregularidades en su actividad eléctrica que puedan estar causando estos episodios. Si los mareos o desmayos ocurren con frecuencia, es crucial someterse a un ECG para descartar problemas cardíacos.
Fatiga inexplicable
La fatiga constante o inexplicable también puede ser un indicio de un problema cardiovascular, especialmente si se acompaña de otros síntomas como hinchazón en las piernas o dificultad para respirar. En tales casos, un electrocardiograma puede ser útil para identificar trastornos como insuficiencia cardíaca, que pueden no ser evidentes sin un examen adecuado.
Chequeos preventivos: La importancia de un ECG regular
Además de los síntomas que mencionamos, existen situaciones en las que un electrocardiograma es recomendable como parte de un chequeo preventivo, especialmente para aquellas personas que tienen antecedentes de enfermedades cardíacas o factores de riesgo.
Antecedentes familiares de enfermedades cardíacas
Si tienes antecedentes familiares de enfermedades del corazón, como infartos, arritmias o insuficiencia cardíaca, es importante realizarse un electrocardiograma regularmente. El ECG puede detectar signos tempranos de afecciones cardíacas hereditarias, lo que permite iniciar un tratamiento preventivo para evitar complicaciones mayores.
Factores de riesgo para problemas cardíacos
El electrocardiograma también es esencial para personas que tienen factores de riesgo conocidos para desarrollar enfermedades cardíacas, como:
- Hipertensión arterial: La presión arterial alta puede dañar las arterias y aumentar el riesgo de enfermedad coronaria y accidentes cerebrovasculares. Un ECG puede ayudar a detectar cualquier afectación del corazón relacionada con la hipertensión.
- Colesterol elevado: Los niveles altos de colesterol LDL (colesterol “malo”) pueden provocar la acumulación de placas en las arterias, lo que aumenta el riesgo de infarto. El ECG puede ayudar a detectar cualquier signo de daño en el corazón debido al colesterol elevado.
- Diabetes: Las personas con diabetes tienen un mayor riesgo de enfermedades del corazón debido a la inflamación y el daño que la hiperglucemia crónica puede causar en los vasos sanguíneos. Realizarse un ECG regularmente es esencial para detectar cualquier problema cardíaco temprano.
Edad avanzada
 Las personas mayores de 60 años tienen un mayor riesgo de sufrir problemas cardíacos. Por ello, se recomienda que, como parte de su control de salud general, se realicen electrocardiogramas de forma periódica, incluso si no presentan síntomas. Un ECG puede detectar alteraciones en el ritmo cardíaco o signos de daño estructural en el corazón, lo que permite iniciar un tratamiento preventivo.
Las personas mayores de 60 años tienen un mayor riesgo de sufrir problemas cardíacos. Por ello, se recomienda que, como parte de su control de salud general, se realicen electrocardiogramas de forma periódica, incluso si no presentan síntomas. Un ECG puede detectar alteraciones en el ritmo cardíaco o signos de daño estructural en el corazón, lo que permite iniciar un tratamiento preventivo.¿Qué esperar durante un electrocardiograma?
El proceso de realizarse un electrocardiograma es rápido, sencillo y no invasivo. Durante el examen, se colocan pequeños electrodos en el pecho, los brazos y las piernas, que captan la actividad eléctrica del corazón. El procedimiento generalmente toma entre 5 y 10 minutos y no causa dolor. Los resultados del ECG se procesan inmediatamente y son revisados por un cardiólogo para identificar cualquier irregularidad.
En resumen
El electrocardiograma es una herramienta diagnóstica fundamental para detectar una amplia variedad de afecciones cardíacas, desde arritmias hasta infartos de miocardio. Es esencial que las personas se realicen un ECG cuando experimenten síntomas como dolor en el pecho, dificultad para respirar, ritmo cardíaco irregular, mareos o fatiga inexplicable. Además, los chequeos preventivos son clave para aquellas personas con factores de riesgo o antecedentes familiares de enfermedades cardíacas. Realizarse un electrocardiograma a tiempo puede marcar la diferencia en la prevención y tratamiento de problemas graves del corazón.
-
¿Cómo interpretar los resultados de un examen general de orina?
SRC:SelfWritten
El examen general de orina es un procedimiento clínico esencial que ofrece una visión completa sobre la salud del paciente. Este análisis, basado en el estudio de diferentes parámetros físicos, químicos y microscópicos, permite identificar alteraciones en el sistema urinario, metabólico o inmunológico. Para muchos pacientes, interpretar los resultados de un examen general de orina puede ser un desafío. En este artículo se explica cómo leer los datos proporcionados y comprender su relevancia clínica.
Principales parámetros en un examen general de orina
El análisis de orina se divide en tres categorías: características físicas, análisis químico y examen microscópico. Cada una proporciona información clave sobre la salud del paciente.
Análisis físico: Aspecto y color de la orina
 El color y la claridad de la orina son las primeras características evaluadas. Una orina de color amarillo claro indica hidratación adecuada, mientras que tonos oscuros pueden señalar deshidratación o la presencia de bilirrubina, asociada a trastornos hepáticos.
El color y la claridad de la orina son las primeras características evaluadas. Una orina de color amarillo claro indica hidratación adecuada, mientras que tonos oscuros pueden señalar deshidratación o la presencia de bilirrubina, asociada a trastornos hepáticos.La turbidez o falta de claridad puede deberse a infecciones urinarias, presencia de cristales o exceso de células. Aunque estos cambios no siempre son graves, deben ser evaluados en conjunto con otros parámetros.
Análisis químico: Parámetros clave
El análisis químico se realiza utilizando tiras reactivas que miden diferentes componentes de la orina. Entre los más relevantes se encuentran:
- Proteínas en orina:
- Normalmente, la orina contiene trazas mínimas de proteínas. La presencia de proteínas (proteinuria) puede ser un indicador de daño renal, hipertensión o infecciones urinarias. Valores elevados requieren evaluación adicional, como análisis de proteínas específicas.
- Glucosa:
- La glucosuria, o glucosa en la orina, suele ser un signo de diabetes mellitus. Si los niveles de glucosa en sangre superan el umbral renal, esta sustancia pasa a la orina. Su presencia requiere confirmación mediante análisis de sangre.
- Cetonas:
- Las cetonas aparecen en la orina cuando el cuerpo utiliza grasas como fuente principal de energía, en lugar de carbohidratos. Esto es común en personas con diabetes mal controlada, en dietas cetogénicas o durante episodios de ayuno prolongado.
- pH:
- El pH urinario indica si la orina es ácida o alcalina. Valores normales oscilan entre 4.5 y 8. Cambios en el pH pueden estar relacionados con infecciones, formación de cálculos renales o alteraciones metabólicas.
- Leucocitos y nitritos:
- La presencia de leucocitos en la orina sugiere una posible infección urinaria. Si se detectan nitritos, es probable que existan bacterias productoras de esta sustancia, lo que refuerza el diagnóstico de infección.
Examen microscópico: Elementos celulares y cristales
El análisis microscópico de la orina permite observar elementos sólidos presentes en la muestra. Estos incluyen:
- Células rojas (eritrocitos): La hematuria, o presencia de sangre en la orina, puede ser un signo de infecciones, cálculos renales o trastornos más serios como tumores.
- Células blancas (leucocitos): Un número elevado refuerza la sospecha de infección.
- Cristales: Indican una posible predisposición a formar cálculos renales. Algunos cristales, como los de ácido úrico o calcio, son normales en pequeñas cantidades, mientras que otros pueden ser patológicos.
Interpretación de resultados anormales
Para interpretar los resultados de un examen general de orina, es necesario entender que no todos los valores fuera del rango normal son indicadores de enfermedad. A continuación, se detallan algunos de los hallazgos más comunes y su posible significado clínico.
Proteinuria: Más allá de lo normal
La detección de proteínas en la orina puede deberse a diversas causas. Una proteinuria leve y transitoria puede ocurrir tras el ejercicio físico intenso o durante episodios febriles. Sin embargo, niveles persistentemente altos pueden ser indicativos de enfermedades como nefritis, diabetes o hipertensión.
Glucosuria y diabetes
La glucosa en la orina, aunque común en personas con diabetes, también puede aparecer en situaciones de estrés extremo o durante el embarazo, conocido como diabetes gestacional. Este hallazgo debe confirmarse con un análisis de sangre para medir la glucosa plasmática en ayuno.
Cetonuria: Energía y metabolismo
La aparición de cetonas en la orina es común en personas que siguen dietas bajas en carbohidratos o durante el ayuno prolongado. En casos de diabetes tipo 1, puede ser un signo de cetoacidosis diabética, una emergencia médica que requiere atención inmediata.
Hematuria: Sangre en la orina
Aunque puede ser visible a simple vista, la hematuria microscópica solo se detecta en el laboratorio. Es fundamental investigar la causa subyacente, que puede variar desde infecciones leves hasta patologías graves como cáncer de vejiga.
Alteraciones del pH y cálculos renales
Un pH ácido puede asociarse a cálculos de ácido úrico, mientras que un pH alcalino favorece la formación de cálculos de fosfato. Además, infecciones urinarias recurrentes pueden alterar el pH, lo que dificulta el tratamiento de estas afecciones.
Factores que influyen en los resultados
Es importante considerar que diversos factores pueden alterar los resultados de un examen de orina. Por ejemplo, una recolección incorrecta de la muestra, el consumo de ciertos medicamentos o incluso la dieta del paciente pueden influir en los valores obtenidos. Por ello, es crucial seguir las indicaciones del médico y realizar un análisis integral que contemple todos los parámetros.
Reflexión final
El análisis de los resultados de un examen general de orina requiere una comprensión detallada de los parámetros evaluados y su posible relación con la salud del paciente. Este procedimiento no solo detecta alteraciones metabólicas y del sistema urinario, sino que también sirve como herramienta preventiva en el diagnóstico temprano de enfermedades graves. Aunque algunos valores pueden parecer alarmantes a primera vista, es fundamental interpretarlos en el contexto clínico del paciente. Un análisis detallado y un seguimiento médico adecuado son esenciales para garantizar un diagnóstico preciso y un tratamiento oportuno.
- Proteínas en orina:
-
¿Cómo se realiza un examen general de orina?
El examen general de orina es una herramienta diagnóstica esencial en la medicina, utilizada para evaluar el estado de salud del paciente y detectar posibles anomalías en el sistema urinario o metabólico. Este procedimiento clínico permite analizar características físicas, químicas y microscópicas de la orina, brindando información relevante para el diagnóstico de enfermedades. A continuación, se detalla cómo se realiza un examen general de orina, incluyendo los pasos de preparación, recolección y análisis.
Preparación del paciente para el examen general de orina
Antes de realizar el análisis, es fundamental que el paciente reciba instrucciones claras sobre la recolección de muestra de orina para garantizar la calidad de los resultados. La preparación incluye los siguientes aspectos:
 Instrucciones dietéticas:
Instrucciones dietéticas:
- Es recomendable que el paciente evite alimentos que puedan alterar las características de la orina, como remolacha, zanahoria o ciertos medicamentos que modifiquen el color o el pH.
- Si está tomando fármacos, debe informar al médico, ya que algunos pueden interferir en el resultado.
- Higiene previa:
- Se debe limpiar adecuadamente la zona genital para evitar la contaminación de la muestra con bacterias o secreciones externas.
- En mujeres, es ideal realizar el procedimiento fuera del periodo menstrual para minimizar posibles contaminantes.
- Momento adecuado para la muestra:
- La primera orina de la mañana es preferible, ya que está más concentrada y permite detectar mejor anomalías.
Recolección de la muestra de orina: Pasos clave
La recolección de muestra de orina es un paso crucial para obtener resultados confiables. Un procedimiento incorrecto puede afectar significativamente el análisis. El protocolo incluye las siguientes etapas:
1. Selección del recipiente:
- Se debe utilizar un contenedor estéril, proporcionado por el laboratorio o el centro médico.
- Es importante no tocar el interior del recipiente para evitar la introducción de contaminantes.
2. Método de recolección:
- La técnica de “chorro medio” es la más común para evitar la contaminación inicial. Esto implica:
- Comenzar a orinar directamente en el inodoro.
- Detener brevemente el flujo y recolectar el siguiente chorro en el recipiente estéril.
- Evitar llenar el recipiente por completo; usualmente, 30-50 ml son suficientes.
3. Almacenamiento y transporte:
- La muestra debe ser entregada al laboratorio en un plazo de 1 a 2 horas para evitar alteraciones en su composición química y microbiológica.
- Si no es posible entregarla de inmediato, debe mantenerse refrigerada entre 2°C y 8°C, aunque esto no es ideal para ciertos análisis específicos.
Protocolo para el análisis de orina
Una vez que la muestra es recibida en el laboratorio, se procede a realizar un análisis detallado, el cual incluye tres componentes principales:
1. Análisis físico:
- Color y aspecto: Se evalúa si la orina es clara, turbia, o presenta colores anormales que puedan indicar infecciones, hematuria o ictericia.
- Olor: Aunque subjetivo, un olor inusual puede ser signo de infecciones o alteraciones metabólicas, como la cetoacidosis diabética.
2. Análisis químico:
- pH: Mide el grado de acidez o alcalinidad, útil para identificar infecciones o trastornos renales.
- Glucosa y cetonas: Presencia asociada a diabetes o metabolismo alterado.
- Proteínas: Indicativo de daño renal o enfermedades sistémicas.
- Leucocitos y nitritos: Indicadores comunes de infección urinaria.
3. Examen microscópico:
- Se realiza para identificar elementos como glóbulos rojos, glóbulos blancos, cristales o bacterias presentes en la muestra.
- La identificación de sedimentos anormales puede señalar infecciones, litiasis o trastornos inflamatorios.
Recomendaciones para obtener resultados precisos
Para garantizar la validez del análisis, tanto el paciente como el personal médico deben seguir medidas específicas:
- Evitar errores comunes en la recolección:
- No utilizar recipientes no estériles o muestras obtenidas después de un tiempo prolongado de recolección.
- Prevenir la contaminación cruzada con sustancias externas.
- Comunicar al médico antecedentes médicos:
- Es esencial informar sobre infecciones recientes, embarazos, uso de medicamentos o procedimientos quirúrgicos que puedan influir en los resultados.
- Cumplir con los tiempos establecidos:
- La frescura de la muestra es determinante. Retrasos en el transporte o almacenamiento incorrecto pueden generar resultados poco confiables.
Importancia del examen general de orina en el diagnóstico médico
El examen general de orina es un procedimiento simple, no invasivo y altamente eficaz para identificar múltiples condiciones de salud. Permite detectar infecciones urinarias, enfermedades renales, trastornos metabólicos como diabetes, y otras anomalías. Su papel como herramienta preventiva es invaluable, ya que muchas patologías pueden ser tratadas eficazmente si se diagnostican a tiempo.
El proceso adecuado, desde la preparación del paciente hasta la entrega de resultados, garantiza la precisión del diagnóstico. Además, la educación al paciente sobre la importancia de seguir las indicaciones del médico es clave para evitar resultados erróneos y reducir la necesidad de repetir el procedimiento.
-
Colposcopia y Diagnóstico del VPH: Lo Que Debes Saber
SRC:SelfWritten
 La colposcopia es un procedimiento esencial en el diagnóstico y seguimiento de infecciones causadas por el Virus del Papiloma Humano (VPH), especialmente aquellas asociadas con alto riesgo oncogénico. Este examen permite detectar lesiones precancerosas en el cuello uterino y establecer un tratamiento oportuno, protegiendo así la salud ginecológica de la mujer. A continuación, exploraremos cómo la colposcopia contribuye al manejo del VPH, su relación con el cáncer cervicouterino y las recomendaciones para quienes reciben un diagnóstico positivo.
La colposcopia es un procedimiento esencial en el diagnóstico y seguimiento de infecciones causadas por el Virus del Papiloma Humano (VPH), especialmente aquellas asociadas con alto riesgo oncogénico. Este examen permite detectar lesiones precancerosas en el cuello uterino y establecer un tratamiento oportuno, protegiendo así la salud ginecológica de la mujer. A continuación, exploraremos cómo la colposcopia contribuye al manejo del VPH, su relación con el cáncer cervicouterino y las recomendaciones para quienes reciben un diagnóstico positivo.¿Qué es el VPH y cómo afecta la salud ginecológica?
El VPH es una infección de transmisión sexual altamente común que afecta a hombres y mujeres. Existen más de 100 tipos de VPH, de los cuales algunos se clasifican como de alto riesgo debido a su capacidad de causar lesiones precancerosas y cáncer cervicouterino. Este virus puede permanecer asintomático durante años, lo que dificulta su detección sin pruebas específicas.
La colposcopia como herramienta diagnóstica del VPH
Detección de lesiones asociadas al VPH
La colposcopia permite observar detalladamente el cuello uterino para identificar cambios anormales en las células epiteliales. Utilizando un colposcopio, el especialista examina el tejido cervical tras la aplicación de soluciones químicas que resaltan áreas sospechosas. Estas lesiones pueden ser indicativas de una infección por VPH, especialmente si se trata de tipos de alto riesgo.
Toma de biopsias durante la colposcopia
Cuando se detectan áreas sospechosas, el médico puede realizar una biopsia dirigida para analizar el tejido en laboratorio. Esto ayuda a confirmar si las células anormales son benignas, precancerosas o cancerosas, proporcionando información crítica para el diagnóstico y tratamiento.
Relación entre el VPH y el cáncer cervicouterino
Cómo el VPH conduce al cáncer
La infección persistente por tipos de VPH de alto riesgo, como el 16 y el 18, puede provocar cambios en las células del cuello uterino, conocidos como displasias. Si no se tratan, estas displasias pueden evolucionar a cáncer cervicouterino, un proceso que puede tardar varios años en desarrollarse.
Importancia de la detección temprana
La colposcopia, junto con pruebas como el Papanicolaou y la detección de ADN del VPH, es fundamental para identificar lesiones en etapas iniciales. Esto permite un tratamiento efectivo antes de que se conviertan en cáncer, mejorando significativamente el pronóstico de la paciente.
¿Qué sucede durante una colposcopia para el diagnóstico del VPH?
El procedimiento es ambulatorio y suele durar entre 15 y 20 minutos. Después de un examen ginecológico básico, el médico utiliza el colposcopio para inspeccionar el cuello uterino. Durante el examen, se aplica una solución de ácido acético o yodo para resaltar las áreas sospechosas. En caso de identificar anomalías, se realiza una biopsia, cuyo resultado es clave para planificar el tratamiento.
Recomendaciones para mujeres con diagnóstico positivo de VPH
Seguimiento médico regular
Es fundamental asistir a las consultas ginecológicas y realizarse las pruebas recomendadas según la evaluación médica. El seguimiento frecuente ayuda a monitorear cualquier cambio en el tejido cervical y a detectar complicaciones a tiempo.
Vacunación contra el VPH
Aunque la vacuna es más efectiva cuando se administra antes del inicio de la vida sexual, también puede beneficiar a mujeres diagnosticadas con VPH al proteger contra otros tipos del virus.
Adopción de un estilo de vida saludable
Mantener un sistema inmunológico fuerte es clave para combatir el VPH. Una dieta equilibrada, ejercicio regular y la reducción del estrés contribuyen a fortalecer las defensas del organismo.
Evitar factores de riesgo
El tabaquismo y las relaciones sexuales sin protección aumentan el riesgo de complicaciones asociadas al VPH. Abandonar estos hábitos puede mejorar la salud ginecológica y reducir la progresión del virus.
Importancia del tratamiento oportuno
Cuando se diagnostican lesiones causadas por el VPH, el tratamiento temprano es crucial. Las opciones pueden incluir procedimientos como la crioterapia, la conización o la escisión electroquirúrgica, dependiendo del grado de la lesión. Estas intervenciones, aunque simples, son fundamentales para prevenir el desarrollo del cáncer cervicouterino.
Impacto emocional del diagnóstico de VPH
Un diagnóstico positivo de VPH puede generar ansiedad y preocupación. Sin embargo, es importante recordar que esta infección es común y que, en la mayoría de los casos, el sistema inmunológico puede eliminar el virus por sí solo. Contar con el apoyo de profesionales médicos y redes de apoyo emocional puede ser de gran ayuda durante este proceso.
Reflexión final
La colposcopia es una herramienta invaluable en la detección y manejo de las infecciones por VPH. Su capacidad para identificar lesiones precancerosas permite intervenir oportunamente y prevenir complicaciones graves, como el cáncer cervicouterino. Las mujeres diagnosticadas con VPH deben mantenerse informadas, seguir las recomendaciones médicas y adoptar medidas de cuidado personal para proteger su salud a largo plazo.
-
Tamiz Neonatal en el Mundo: Mejores Prácticas y Avances
SRC:SelfWritten
El tamiz neonatal es una herramienta crucial en la detección temprana de enfermedades congénitas y metabólicas. Aunque su implementación varía entre países, las mejores prácticas y avances tecnológicos han permitido salvar millones de vidas y mejorar la calidad de vida de los recién nacidos. Este artículo explora los países con los programas más avanzados, las enfermedades incluidas en sus paneles de detección, y las innovaciones recientes que están revolucionando estas pruebas.
Países con las Mejores Prácticas en Tamiz Neonatal
 La implementación del tamiz neonatal depende en gran medida de la infraestructura sanitaria y las políticas públicas de cada país. Algunos han destacado por sus programas avanzados y la cobertura universal que ofrecen.
La implementación del tamiz neonatal depende en gran medida de la infraestructura sanitaria y las políticas públicas de cada país. Algunos han destacado por sus programas avanzados y la cobertura universal que ofrecen.Estados Unidos
En Estados Unidos, el tamiz neonatal es obligatorio en todos los estados y tiene uno de los paneles de detección más amplios del mundo. Este incluye más de 30 enfermedades metabólicas, endocrinas y genéticas. Gracias a la Ley de Mejora del Tamiz Neonatal (2008), se garantiza la cobertura de estas pruebas en hospitales públicos y privados, lo que permite detectar condiciones raras y tratarlas antes de que se manifiesten clínicamente.
Japón
Japón es reconocido por su enfoque integral y tecnología avanzada en tamiz neonatal. Su programa incluye enfermedades como la fenilcetonuria, la galactosemia y diversas acidemias orgánicas. Además, el país ha desarrollado tecnologías de secuenciación genética que complementan las pruebas estándar, mejorando la precisión y el alcance del diagnóstico.
Suecia
Suecia tiene uno de los programas más completos y equitativos. El tamiz neonatal incluye 25 enfermedades y es gratuito para todos los recién nacidos. Además, el país cuenta con una infraestructura que garantiza la entrega de resultados en menos de 72 horas, permitiendo iniciar tratamientos de forma inmediata cuando es necesario.
Australia
Australia destaca por su enfoque regionalizado, que adapta los paneles de tamiz neonatal según las necesidades de las comunidades. Esto incluye la detección de enfermedades más prevalentes en poblaciones indígenas. Su programa también incorpora pruebas para detectar inmunodeficiencias primarias, lo que es un avance importante en la prevención de enfermedades graves en los primeros meses de vida.
Enfermedades Incluidas en los Paneles de Detección
El alcance de las enfermedades detectadas en el tamiz neonatal varía según el país, pero existen algunas condiciones comúnmente incluidas debido a su alta relevancia clínica.
Fenilcetonuria (PKU)
Presente en casi todos los programas, esta enfermedad metabólica impide al cuerpo procesar la fenilalanina. Si no se trata, puede causar daño cerebral severo. El diagnóstico temprano permite manejarla con una dieta especial.
Hipotiroidismo Congénito
Una de las condiciones más comunes detectadas, el hipotiroidismo congénito puede llevar a retrasos en el desarrollo físico y mental si no se trata a tiempo. La administración de hormonas tiroideas corrige el déficit y asegura un crecimiento normal.
Fibrosis Quística
Esta enfermedad genética afecta principalmente los pulmones y el sistema digestivo. Los paneles avanzados incluyen pruebas que permiten un diagnóstico precoz, mejorando las opciones de tratamiento y la calidad de vida del paciente.
Enfermedades Metabólicas Raras
Muchas naciones han expandido sus paneles para incluir acidemias orgánicas, enfermedades del ciclo de la urea y trastornos mitocondriales. Estas condiciones pueden ser fatales si no se diagnostican a tiempo, pero son tratables mediante dietas especializadas y suplementos.
Inmunodeficiencias Primarias
Programas pioneros, como los de Estados Unidos y Australia, han comenzado a incluir pruebas para detectar inmunodeficiencias, como el síndrome de inmunodeficiencia combinada grave (SCID). Esto permite iniciar tratamientos como trasplantes de médula ósea antes de que surjan complicaciones graves.
Innovaciones Recientes en Pruebas de Tamiz Neonatal
El desarrollo tecnológico ha impulsado avances significativos en el tamiz neonatal, ampliando su alcance y mejorando su precisión.
Secuenciación Genética
La incorporación de tecnologías de secuenciación genética ha permitido identificar enfermedades hereditarias que antes no eran detectables mediante métodos convencionales. Países como Japón y Alemania lideran esta innovación, utilizando pruebas genómicas para personalizar los tratamientos.
Análisis de Espectrometría de Masas
Este método ha revolucionado el tamiz neonatal al permitir la detección simultánea de múltiples enfermedades metabólicas a partir de una sola muestra de sangre. Su implementación ha reducido los costos y mejorado la eficiencia de los programas de detección.
Inteligencia Artificial en el Análisis de Datos
La inteligencia artificial (IA) está comenzando a desempeñar un papel crucial en el análisis de resultados de tamiz neonatal. Algoritmos avanzados ayudan a identificar patrones que podrían indicar la presencia de enfermedades raras, reduciendo los falsos positivos y mejorando la precisión.
Pruebas de Diagnóstico Ampliadas
Algunos países están probando paneles ampliados que incluyen enfermedades raras pero tratables, como la atrofia muscular espinal. Este enfoque permite abordar condiciones que antes no se consideraban viables para el tamiz neonatal debido a limitaciones tecnológicas.
Programas de Tamiz Universal
La implementación de programas de tamiz neonatal universal en regiones con recursos limitados es otra innovación destacada. A través de asociaciones internacionales y financiamiento externo, países en desarrollo están adoptando tecnologías avanzadas para ofrecer cobertura a poblaciones vulnerables.
El Impacto del Tamiz Neonatal en la Salud Global
El tamiz neonatal es una herramienta invaluable que no solo salva vidas, sino que también mejora la calidad de vida de millones de personas en todo el mundo. Los países que han implementado programas avanzados y equitativos han demostrado que la detección temprana puede prevenir complicaciones graves, reducir costos en atención médica y promover el bienestar social.
A medida que las tecnologías avanzan y los programas se expanden, es fundamental garantizar que estas innovaciones sean accesibles para todas las poblaciones. La colaboración internacional y el intercambio de mejores prácticas desempeñan un papel clave en la construcción de sistemas de tamiz neonatal más efectivos y equitativos.
En última instancia, la inversión en el tamiz neonatal no solo beneficia a los recién nacidos y sus familias, sino que también fortalece los sistemas de salud y contribuye al desarrollo sostenible de las comunidades. Al combinar las mejores prácticas, la tecnología de punta y el compromiso político, el tamiz neonatal continuará siendo una de las intervenciones médicas más impactantes del siglo XXI.
-
¿Qué Indica Cada Parámetro en una Biometría Hemática?
SRC:SelfWritten
 La biometría hemática es uno de los análisis más comunes y esenciales en la práctica médica. Este estudio proporciona una evaluación detallada de los componentes celulares de la sangre, lo que ayuda a diagnosticar diversas condiciones de salud. Los tres grupos principales de células sanguíneas analizadas en una biometría hemática son los glóbulos rojos, los glóbulos blancos y las plaquetas. Cada uno de estos grupos tiene parámetros específicos que son fundamentales para entender el estado de salud del paciente. A continuación, se describe qué indican los principales parámetros de una biometría hemática y cómo interpretar sus resultados.
La biometría hemática es uno de los análisis más comunes y esenciales en la práctica médica. Este estudio proporciona una evaluación detallada de los componentes celulares de la sangre, lo que ayuda a diagnosticar diversas condiciones de salud. Los tres grupos principales de células sanguíneas analizadas en una biometría hemática son los glóbulos rojos, los glóbulos blancos y las plaquetas. Cada uno de estos grupos tiene parámetros específicos que son fundamentales para entender el estado de salud del paciente. A continuación, se describe qué indican los principales parámetros de una biometría hemática y cómo interpretar sus resultados.Glóbulos Rojos (Hematocrito y Hemoglobina)
Los glóbulos rojos son células encargadas de transportar oxígeno desde los pulmones hacia el resto del cuerpo y de llevar dióxido de carbono de regreso a los pulmones para su eliminación. Existen dos parámetros fundamentales para evaluar los glóbulos rojos: el hematocrito y la hemoglobina.
Hematocrito
El hematocrito mide el porcentaje de glóbulos rojos en relación con el volumen total de sangre. Es un indicador clave de la capacidad de transporte de oxígeno del cuerpo. Los valores normales varían según el sexo y la edad del paciente. En adultos, los rangos de referencia son aproximadamente:
- Hombres: 40-54%
- Mujeres: 37-47%
Valores bajos de hematocrito pueden indicar anemia, una condición en la que hay una reducción en la capacidad del cuerpo para transportar oxígeno. Esto puede deberse a varias causas, como deficiencia de hierro, pérdida de sangre o enfermedades crónicas. Por otro lado, un hematocrito elevado puede estar relacionado con deshidratación o con enfermedades como la policitemia vera, una patología que provoca un aumento excesivo en la producción de glóbulos rojos.
Hemoglobina
La hemoglobina es una proteína presente en los glóbulos rojos que se une al oxígeno para transportarlo a través de la sangre. Los valores normales de hemoglobina son similares a los del hematocrito, y también varían según el sexo:
- Hombres: 13.8-17.2 g/dL
- Mujeres: 12.1-15.1 g/dL
Una hemoglobina baja, al igual que el hematocrito, es un signo de anemia. La gravedad de la anemia puede clasificarse según los niveles de hemoglobina. Una disminución significativa en los niveles de hemoglobina puede llevar a síntomas como fatiga, debilidad y dificultad para respirar. En contraste, una hemoglobina elevada puede sugerir deshidratación o trastornos como la policitemia.
Glóbulos Blancos (Conteo Total y Diferencial)
Los glóbulos blancos, o leucocitos, son células del sistema inmunológico responsables de combatir infecciones, defender al cuerpo contra agentes extraños y eliminar células dañadas. Una biometría hemática incluye tanto el conteo total de glóbulos blancos como un conteo diferencial, que mide los subtipos específicos de leucocitos.
Conteo Total de Glóbulos Blancos
El conteo total de glóbulos blancos es la cantidad total de leucocitos presentes en un microlitro de sangre. Los valores normales oscilan entre 4,500 y 11,000 células por microlitro. Un aumento en el número de glóbulos blancos (leucocitosis) puede ser un indicativo de infecciones, inflamaciones, estrés, o incluso de ciertos tipos de cáncer, como la leucemia. Por otro lado, una reducción en los glóbulos blancos (leucopenia) puede estar asociada con infecciones virales, enfermedades autoinmunes o efectos secundarios de ciertos medicamentos, como la quimioterapia.
Conteo Diferencial de Glóbulos Blancos
El conteo diferencial divide los glóbulos blancos en sus diferentes tipos: neutrófilos, linfocitos, monocitos, eosinófilos y basófilos. Cada uno de estos subtipos tiene funciones específicas dentro del sistema inmune.
- Neutrófilos: Constituyen entre el 40% y 70% de los glóbulos blancos y son los primeros en responder a infecciones bacterianas. Un aumento de neutrófilos (neutrofilia) puede indicar una infección bacteriana aguda, mientras que un nivel bajo (neutropenia) puede ser un signo de infecciones graves o del uso de medicamentos inmunosupresores.
- Linfocitos: Representan entre el 20% y 40% de los glóbulos blancos. Son fundamentales en la defensa contra infecciones virales y la producción de anticuerpos. Un incremento de linfocitos (linfocitosis) puede señalar una infección viral, mientras que una disminución (linfopenia) puede ser indicativa de inmunodeficiencia o tratamiento con corticosteroides.
- Monocitos: Constituyen entre el 2% y 8% de los glóbulos blancos y se encargan de eliminar desechos celulares y combatir infecciones crónicas. Un aumento en monocitos (monocitosis) puede estar asociado con infecciones crónicas, mientras que un nivel bajo es menos común y generalmente no es clínicamente significativo.
- Eosinófilos: Representan entre el 1% y 4% del total de glóbulos blancos. Están involucrados en la respuesta a infecciones parasitarias y en reacciones alérgicas. Un aumento de eosinófilos (eosinofilia) puede indicar alergias, asma o infecciones parasitarias.
- Basófilos: Son los glóbulos blancos menos abundantes, representando menos del 1%. Están relacionados con las respuestas inflamatorias y alérgicas. Un aumento de basófilos (basofilia) puede estar asociado con alergias, inflamaciones crónicas o ciertos trastornos sanguíneos.
Plaquetas
Las plaquetas, o trombocitos, son células responsables de la coagulación sanguínea. Un recuento adecuado de plaquetas es crucial para evitar hemorragias o trombosis. El rango normal de plaquetas es de 150,000 a 450,000 por microlitro de sangre.
Trombocitopenia
La trombocitopenia es una condición en la que los niveles de plaquetas están por debajo del rango normal. Puede ser causada por enfermedades autoinmunes, infecciones virales, deficiencia de vitamina B12 o el uso de ciertos medicamentos, como los anticoagulantes. La trombocitopenia grave puede resultar en un mayor riesgo de sangrado espontáneo y moratones.
Trombocitosis
En contraste, la trombocitosis se refiere a un exceso de plaquetas en la sangre. Esto puede estar relacionado con enfermedades inflamatorias, infecciones o trastornos mieloproliferativos, que son enfermedades en las que la médula ósea produce demasiadas células sanguíneas. La trombocitosis puede aumentar el riesgo de formación de coágulos, lo que puede llevar a eventos como trombosis venosa profunda o embolias pulmonares.
Análisis Final
La biometría hemática es una herramienta crucial para evaluar la salud general y detectar condiciones subyacentes. Los resultados de este análisis ofrecen una visión clara del funcionamiento del cuerpo en cuanto a la producción y regulación de células sanguíneas. Cada parámetro proporciona información valiosa sobre el estado del sistema inmunológico, la capacidad de transporte de oxígeno y la función de coagulación. Interpretar correctamente los resultados puede ayudar a los profesionales médicos a realizar diagnósticos precisos y a proponer tratamientos adecuados para mejorar la salud del paciente.
-
Relación entre Biometría Hemática y Enfermedades Autoinmunes
SRC:SelfWritten
La biometría hemática es una herramienta esencial para evaluar el estado general de salud y detectar anomalías en los componentes de la sangre. Además de identificar enfermedades comunes como anemia e infecciones, este análisis puede ser clave para detectar alteraciones que indiquen la presencia de enfermedades autoinmunes. Estas patologías, en las que el sistema inmunitario ataca tejidos sanos del propio cuerpo, suelen manifestarse con cambios en parámetros como los glóbulos blancos y las plaquetas.Alteraciones en glóbulos blancos y plaquetas en enfermedades autoinmunes
Los glóbulos blancos y las plaquetas desempeñan un papel crucial en la defensa del organismo y en la coagulación sanguínea, respectivamente. Las enfermedades autoinmunes suelen causar desequilibrios en estos componentes, lo que puede ser detectado mediante una biometría hemática.
Glóbulos blancos
El recuento de glóbulos blancos puede verse afectado de diversas maneras según la enfermedad autoinmune:
- Leucocitosis (aumento de glóbulos blancos): Puede observarse en etapas inflamatorias de enfermedades como el lupus eritematoso sistémico. Este incremento refleja la respuesta del sistema inmunitario frente a la inflamación crónica.
- Leucopenia (disminución de glóbulos blancos): Es común en pacientes con lupus, donde los mecanismos autoinmunes pueden atacar las células blancas, reduciendo su número.
La variación en subtipos específicos de leucocitos, como linfocitos y neutrófilos, también proporciona información valiosa. Por ejemplo, en el lupus, la linfopenia (disminución de linfocitos) es un hallazgo frecuente.
Plaquetas
Las alteraciones en el recuento de plaquetas son características de varias enfermedades autoinmunes:
- Trombocitopenia (bajo recuento de plaquetas): Es común en trastornos como el lupus o el síndrome antifosfolípido, donde los anticuerpos atacan las plaquetas o interfieren en su producción. Esto puede aumentar el riesgo de hemorragias.
- Trombocitosis (aumento de plaquetas): Aunque menos frecuente, puede presentarse en condiciones inflamatorias crónicas como la artritis reumatoide, reflejando un estado de inflamación sistémica.
Casos comunes de enfermedades autoinmunes detectadas mediante biometría hemática
La biometría hemática es una herramienta valiosa para la detección y el seguimiento de enfermedades autoinmunes. A continuación, se describen dos casos comunes donde este estudio juega un papel fundamental.
Lupus eritematoso sistémico
El lupus es una enfermedad autoinmune que afecta múltiples órganos y sistemas. En la biometría hemática, suelen observarse:
- Anemia: Una disminución de los glóbulos rojos, frecuente en el lupus, puede deberse a inflamación crónica, deficiencias nutricionales o la presencia de anticuerpos contra los eritrocitos.
- Leucopenia: La reducción de leucocitos, especialmente linfocitos, es un marcador común en pacientes con lupus activo.
- Trombocitopenia: El recuento bajo de plaquetas puede deberse a la destrucción mediada por anticuerpos, lo que aumenta el riesgo de hemorragias.
La detección de estas alteraciones es clave para iniciar un diagnóstico temprano y determinar la actividad de la enfermedad, lo que permite ajustar el tratamiento según las necesidades del paciente.
Artritis reumatoide
La artritis reumatoide es un trastorno autoinmune caracterizado por inflamación crónica de las articulaciones. La biometría hemática puede revelar los siguientes cambios:
- Anemia de enfermedad crónica: La inflamación persistente puede reducir la producción de glóbulos rojos, causando una anemia leve a moderada.
- Leucocitosis: En etapas agudas de inflamación, los glóbulos blancos pueden aumentar como respuesta del cuerpo.
- Trombocitosis: Un recuento elevado de plaquetas es frecuente debido al estado inflamatorio asociado con esta enfermedad.
Estos parámetros, combinados con otros estudios específicos como la velocidad de sedimentación globular y los niveles de proteína C reactiva, ayudan a evaluar la severidad de la artritis reumatoide y la eficacia del tratamiento.
Recomendaciones para el seguimiento de enfermedades autoinmunes
El monitoreo regular mediante biometría hemática es esencial para gestionar enfermedades autoinmunes de manera efectiva. A continuación, se destacan algunas recomendaciones clave para el seguimiento:
Control periódico
Realizar biometrías hemáticas regulares permite detectar cambios en los parámetros sanguíneos que indiquen progresión o remisión de la enfermedad. Esto es especialmente importante en pacientes bajo tratamiento inmunosupresor, ya que estos medicamentos pueden afectar los glóbulos blancos y las plaquetas.
Interpretación en contexto clínico
Los resultados de la biometría hemática deben interpretarse en conjunto con la historia clínica, los síntomas del paciente y otros estudios complementarios, como pruebas de autoanticuerpos. Esto asegura un diagnóstico preciso y evita interpretaciones erróneas.
Ajuste del tratamiento
La biometría hemática proporciona información valiosa sobre la respuesta del paciente al tratamiento. Por ejemplo, una mejora en los niveles de hemoglobina o plaquetas puede indicar eficacia del tratamiento, mientras que una disminución en leucocitos podría sugerir la necesidad de ajustar la dosis de medicamentos inmunosupresores.
Prevención de complicaciones
El seguimiento cercano de los parámetros sanguíneos ayuda a prevenir complicaciones graves, como infecciones en pacientes con leucopenia o hemorragias en aquellos con trombocitopenia. Esto permite intervenir de manera oportuna para proteger la salud del paciente.
Análisis final
La biometría hemática es una herramienta invaluable en la detección y el manejo de enfermedades autoinmunes. Su capacidad para identificar alteraciones en glóbulos blancos, glóbulos rojos y plaquetas la convierte en una prueba esencial para el diagnóstico temprano y el seguimiento continuo de patologías como el lupus eritematoso sistémico y la artritis reumatoide. Además de facilitar el ajuste del tratamiento, este análisis permite prevenir complicaciones graves asociadas con estas enfermedades. Su uso regular y la interpretación adecuada en el contexto clínico son fundamentales para mejorar la calidad de vida de los pacientes y optimizar los resultados terapéuticos.

-
Subscribe
Subscribed
Already have a WordPress.com account? Log in now.